
Bioactief composiet ondersteunt de genezing van botbreuken
Botbreuken die niet genezen kunnen een enorme belasting zijn voor patiënten. Ze leiden vaak tot nog meer chirurgische ingrepen. Daardoor vormen ze een uitdaging voor traumachirurgie. Samen met partners hebben Fraunhofer-onderzoekers een composietmateriaal ontwikkeld voor gebruik in de operatiekamer. Dit zou het succes van de behandeling aanzienlijk moeten verbeteren en een snellere genezing mogelijk moeten maken.
Het materiaal bestaat uit een combinatie van een biologisch afbreekbaar polymeer en bioactief glas dient als een sturende of ondersteunende implantaat – scaffold genoemd – om botbreuken sneller te genezen. Het doel is om de groei van bacteriën op de plaats de wond te remmen en de groei van nieuwe botsubstantie te bevorderen. De innovatieve medische technologie is ontwikkeld als onderdeel van het gezamenlijke SCABAEGO-project. Dit wordt gefinancierd door het Duitse Federale Ministerie van Onderwijs en Onderzoek (BMBF). Het Fraunhofer Institute for Manufacturing Technology and Advanced Materials IFAM zal het eerste demonstratiemodel tonen op de COMPAMED medische technologiebeurs in Düsseldorf.
Elegante en effectieve oplossing
Het Fraunhofer IFAM in Bremen presenteert nu een elegante en effectieve oplossing in het gezamenlijke project SCABAEGO (Scaffold bio-active glass enhanced osteogenesis). Het doel van het project is het testen van de werkhypothese dat het gebruik van bioactieve materialen tijdens chirurgie het genezingsproces ondersteunt en het infectierisico vermindert. De Kliniek voor Trauma- en Reconstructieve Chirurgie van het Universitair Ziekenhuis Heidelberg en BellaSeno GmbH, een specialist in medische technologie uit Leipzig, zijn als partners betrokken.
Botbreuken onder de loep
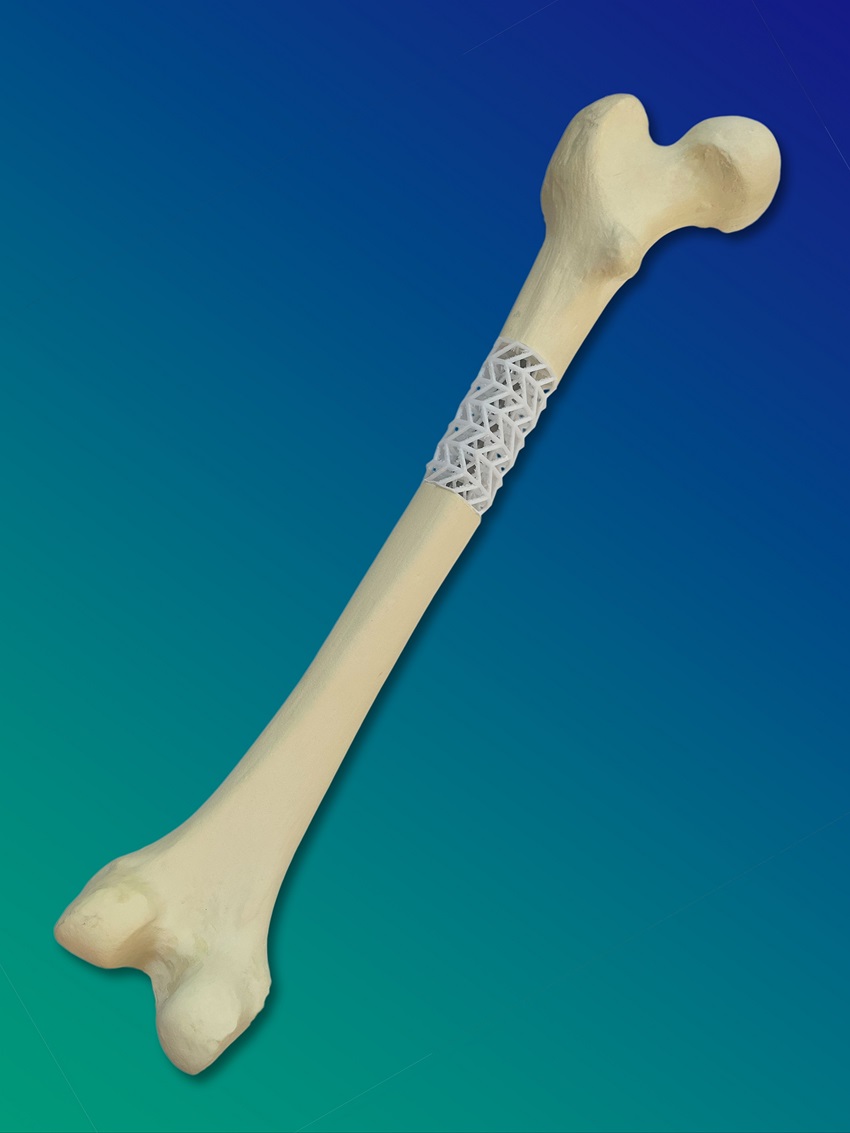
De onderzoekers van Fraunhofer IFAM hebben een composietmateriaal ontwikkeld van het biologisch afbreekbare polymeer polycaprolacton (PCL) en bioactief glas. Dit composiet wordt vervolgens gebruikt voor het 3D-printen van aangepaste hoofd- en ondersteunende structuren voor botbreuken, zogenaamde scaffolds. Hieraan voorafgaand wordt de structuur van het beschadigde bot in kaart gebracht met behulp van computertomografie (CT). De op maat gemaakte structuur vervangt het ontbrekende deel van het bot. De structuur wordt vervolgens gevuld met beenmerg afkomstig van de bekkenkam of van grotere lange botten. Dit zorgt ervoor dat het biologische botvervangingsmateriaal stabiel op zijn plaats blijft en dat de breuklocatie veilig geneest.
Lager risico op infecties
Het innovatieve medische hulpmiddel biedt nog meer voordelen. “Het bioactieve glas in de scaffold verhoogt de pH-waarde van de omgeving naar het basische bereik. Vervolgens willen we de verwachte remming van bacteriële groei onderzoeken,” legt Dr. Kai Borcherding uit. Hij is hoofd van de Business Unit Medische Technologie en Levenswetenschappen bij Fraunhofer IFAM. De onderzoekers verwachten dat dit het risico op infecties na een operatie aanzienlijk zal verminderen.
Bioactief composietmateriaal verandert in bot
Bovendien bevordert bioactief glas de vorming van nieuwe botsubstantie op de plaats van de breuk. Dit komt doordat het glas in contact met lichaamsvloeistoffen verandert in hydroxyapatiet, een chemische verbinding die voornamelijk bestaat uit calciumfosfaat, een stof die dicht bij het bot staat. “Met bioactief glas kunnen de klinisch relevante problemen worden aangepakt – remming van bacteriële groei en effectieve ondersteuning van botgenezing. Na zes of zeven jaar is de scaffold ook volledig afgebroken of omgezet in botsubstantie,” zegt traumachirurg PD Dr Tobias Großner. Hij is hoofdarts en hoofd van de afdeling Experimentele Traumachirurgie aan het Universitair Ziekenhuis Heidelberg.
Niet helemaal nieuw
Het bioactieve glas wordt al gebruikt om botdefecten te behandelen. Nieuw is echter de combinatie met PCL op industriële schaal. De Fraunhofer-onderzoekers zijn erin geslaagd glas en PCL te combineren tot een composietmateriaal dat direct kan worden gebruikt in 3D-productie. Dit maakt het mogelijk om met name patiëntspecifieke 3D-scaffolds te realiseren. Het composietmateriaal kan snel en eenvoudig op industriële schaal worden geproduceerd. “Het PCL polymeer wordt gemengd met het glasgranulaat en een oplosmiddel en vervolgens in verschillende stappen verwerkt. Uiteindelijk wordt het oplosmiddel verwijderd door te drogen en wordt het overgebleven composiet fijn gegranuleerd,” legt Borcherding uit.
Nieuw concept voor ongecompliceerde genezing
Vergeleken met conventionele procedures zou het innovatieve composietmateriaal een aanzienlijke vooruitgang in de behandeling mogelijk moeten maken. Voorheen werd de plaats van de breuk tijdens een eerste operatie bedekt met botcement. Het menselijk organisme ziet het cement als een vreemd lichaam en omhult het met nieuw periost (membraan van Masquelet). Dit proces duurt tot twee maanden. Daarna moet de patiënt terug naar de operatiekamer. Daar snijdt de chirurg het periosteum open, verwijdert het cement, vult de autologe botsubstantie op die van een andere plaats is genomen en hecht het periosteum opnieuw. Tot nu toe waren er slechts beperkte mogelijkheden om de zachte botsubstantie stevig te verankeren en zo een ongestoorde genezing te bereiken. In combinatie met een plaat of nagel biedt de scaffold de zachte botsubstantie de nodige ondersteuning totdat het bot genezen is.
Openingsfoto: Van PCL (links) naar composiet (rechts), gevuld met bioactief glas (midden). (Foto: Fraunhofer IFAM)
Lees ook: 3D-geprint implantaat maakt herstel van versleten pols mogelijk
Meer nieuws
Onderzoekers van QIA ontwikkelen eerste besturingssysteem voor quantumnetwerken

(productnews)
High tech / 17-03-2025
Lees meerFoundation model van Backflip AI vereenvoudigt omzetten van 3D-scan in 3D-model

(productnews)
High tech / 17-03-2025
Lees meerNVDE over onderzoek netkosten: investeringen noodzakelijk voor toekomstbestendige economie

(productnews)
Energie / 14-03-2025
Lees meerZweedse accufabrikant Northvolt vraagt faillissement aan
